前臨床CROの世界市場は2033年までに113億ドルに達する見込み - IMARC Group
グローバル前臨床CRO市場の統計、見通し、地域分析 2025年~2033年
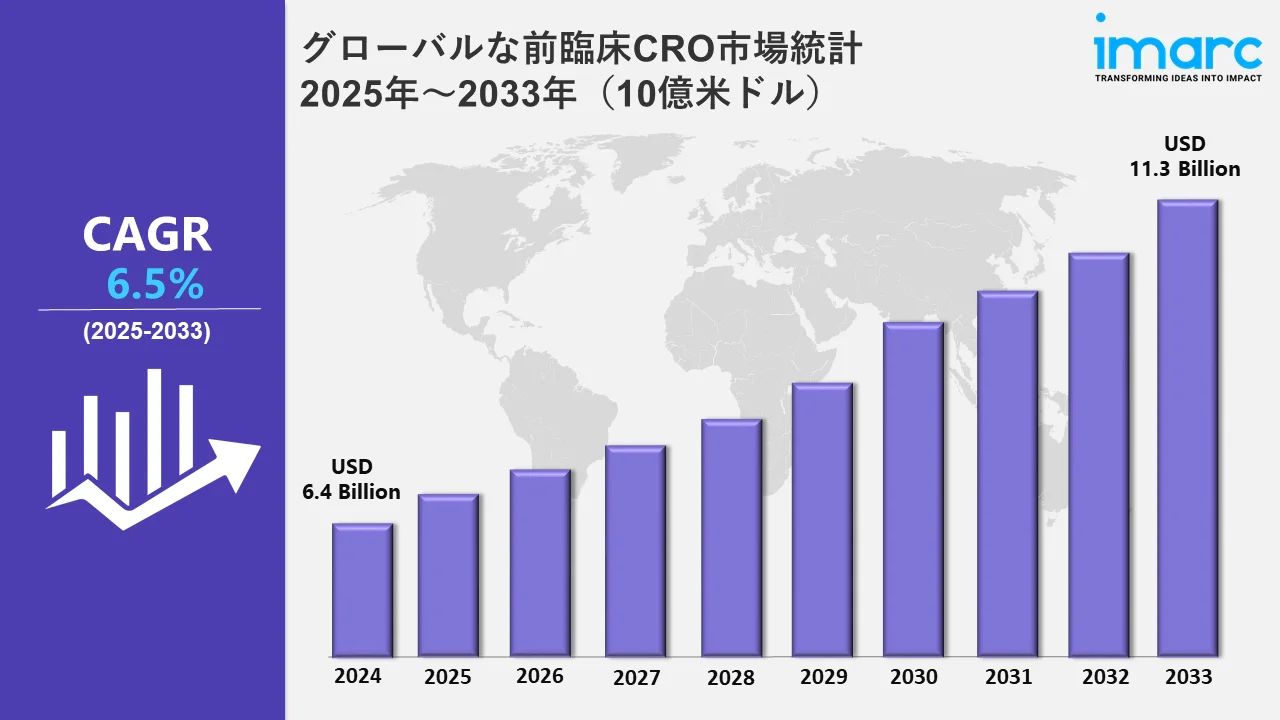
グローバル前臨床CRO市場規模は2024年に64億米ドルと評価され、2033年には113億米ドルに達すると予想され、2025年から2033年までの成長率(CAGR)は6.5%である。
この市場に関するより詳細な情報を得るには, サンプル請求
費用対効果に優れた効率的な創薬プロセスの需要が高まっていることを受け、前臨床試験の CRO 市場は成長しています。そのため、製薬会社やバイオテクノロジー企業は前臨床研究を専門機関に委託するようになっています。 また、薬物開発の複雑化に伴い、毒物学、薬理学、ADME 研究におけるより高度な専門性が求められるようになっていることも、アウトソーシングの傾向を後押ししています。 完全な前臨床評価の必要性を強調する規制要件により、グローバルスタンダードを満たす CRO の役割はより明確なものとなっています。例えば、2024年7月11日、サテロス・バイオサイエンスは、筋肉再生のための低分子薬SAT-3247の臨床研究提案を、グローバルな規制基準を満たす前臨床研究を裏付けとして、TGAのCTNスキームのもと、オーストラリアのHRECに提出しました。また、生物製剤や個別化医療への注目が高まっていることから、遺伝子治療や細胞治療などの新たな治療法に合わせた前臨床サービスの需要が高まっています。一方で、AI主導の研究デザインにおけるイノベーションにより、CROとの提携が強化されています。
医薬品研究開発(R&D)活動の世界的な拡大、特に新興市場における拡大が、前臨床 CRO セクターの成長を大きく後押ししている。慢性疾患の有病率の上昇と革新的な治療に対する需要の増加は、前臨床サービスの必要性をさらに高めている。インシリコモデリング、3D 細胞培養システム、臓器オンチッププラットフォームなどの先端技術は、前臨床試験の質と予測精度を高め、創薬におけるその役割を確固たるものにしている。例えば、2024年9月24日、Hesperos’ Human-on-a-Chip技術は、Dianthus Therapeutics’の全身型重症筋無力症を対象としたDNTH103の第II相試験のFDA申請をサポートし、神経伝達を改善し筋肉疲労を軽減する臓器オンチップ技術の有効性を実証した。CROと学術機関のコラボレーションは、最先端のイノベーションを推進し続け、医薬品開発プロセスにおけるCROの不可欠性を強化し、前臨床研究手法の進歩をさらに加速させています。
前臨床CROの世界市場統計、地域別
この市場調査レポートは、北米(米国、カナダ)、アジア太平洋(中国、日本、インド、韓国、オーストラリア、インドネシア、その他)、欧州(ドイツ、フランス、英国、イタリア、スペイン、ロシア、その他)、中南米(ブラジル、メキシコ、その他)、中東・アフリカを含むすべての主要地域市場についても包括的な分析を提供している。報告書によると、北米 先進的な研究インフラ、大規模な医薬品投資、熟練した専門家、学界と産業界の強力な協力関係が最大の市場シェアを占めている。
北米の前臨床CRO市場の動向:
北米は、高度な研究インフラ、高い研究開発投資、大手製薬会社やバイオテクノロジー企業の広範な存在により、前臨床 CRO 市場をリードしています。この地域では、学術界と産業界の強力な連携により、創薬におけるイノベーションが促進されています。さらに、コストと期間を削減するための前臨床試験のアウトソーシングへの注目が高まっていることも、市場の成長を後押ししています。また、医薬品開発イニシアティブに対する規制当局の支援や政府の資金援助も、この地域の市場拡大に貢献しています。例えば、2024年8月7日、Bruker Corporationは、欧米における生物物理学的手段および技術の進歩を目的として、創薬に特化した前臨床 CRO である NovAliX に出資しました。この提携は、Bruker の NMR、バイオセンサー、質量分析の専門知識を活用して NovAliX のサービスを強化し、創薬と新薬開発におけるイノベーションを促進することを目的としています。
アジア太平洋地域の前臨床 CRO 市場動向:
アジア太平洋地域の前臨床 CRO 市場は、低コストのサービス提供、研究開 発への高額の投資、製薬産業の改善によって促進されていることを考慮すると、 非常に急速に発展している。この地域の国々は、非常に近代化された研究室構造を持つ高度に有能な人材を擁しているため、重要な拠点として浮上している。慢性疾患の症例が増加し、その他の必要条件から、企業はこの地域で前臨床研究のアウトソーシングを求めるようになるだろう。好ましい規制改革と政府の支援は、市場の成長をさらに増大させる。
欧州前臨床 CRO 市場動向:
強力な製薬部門と医薬品開発に対する厳しい規制要件に支えられ、欧州が市場で大きなシェアを占めている。この地域は精密医療とバイオテクノロジーの革新に重点を置いており、前臨床サービスの需要を牽引している。ドイツ、英国、フランスなどの国々は、その高度な研究能力により市場をリードしている。さらに、前臨床試験のアウトソーシングが増加し、運営コストの削減と効率化が図られていることも、欧州地域全体の市場成長に寄与している。
ラテンアメリカの前臨床 CRO 市場動向:
着実に発展しているラテンアメリカ市場の特徴は、急成長する製薬部門と臨床研究活動の活発化である。研究インフラが強化されたブラジルとメキシコは、こうした発展の始まりを示す一方、研究開発に対する政府の支援により、この地域でのビジネスチャンスが拡大している。費用対効果の高いソリューションに対する需要の高まりも、グローバル企業をこの地域に向かわせる原動力となっている。さらに、慢性疾患の増加と革新的な医薬品開発への関心の高まりが、この市場を後押ししている。
中東およびアフリカの前臨床CRO市場動向:
中東およびアフリカでは、特に南アフリカやアラブ首長国連邦(UAE)などの国々において、ヘルスケアインフラの改善と製薬研究能力の向上が重視される傾向が強まっており、前臨床試験 CRO 市場は徐々に成長しています。 また、グローバルな協力体制と投資が前臨床研究能力の研究基盤の開発を促進していることも、この地域の市場の潜在的な成長要因となっています。 医薬品開発と新療法における費用対効果の高いソリューションに対する需要の高まりも、この地域の市場の潜在的な成長要因となっています。
前臨床CRO業界をリードするトップ企業
前臨床CRO市場の大手企業には Charles River Laboratories Inc., Covance Inc. (Laboratory Corporation of America Holdings), Eurofins Scientific, ICON Plc, MD Biosciences Inc. (MLM Medical Labs), Medpace, Parexel International Corporation, PPD Inc., と Wuxi AppTec, などがある。2024年2月21日、チャールズ・リバー・ラボラトリーズとウィーラー・バイオは、ウィーラーのポータブルCMCプラットフォームを通じて前臨床から臨床への移行を加速するために提携した。この提携により、チャールズ・リバー社の抗体創製の専門知識とウィーラー社の高度なCMC能力が統合され、初期段階のバイオテクノロジー企業のタイムラインと複雑さが軽減されます。Wheeler社のCGMP対応施設とモジュール式ワークフローは、高品質で安価な臨床製剤の製造をサポートします。この提携により、前臨床CROおよびCDMOサービスが効率化され、創薬が最適化され、ヒト初臨床試験への迅速な移行が可能になります。
世界の前臨床CRO市場のセグメンテーション範囲
- サービス別に見ると、バイオアナリシスとDMPK試験、毒物学試験、その他に分類される。毒性試験分野は、医薬品、化学物質、その他の物質がヒトに暴露される前にその安全性を確認するという重要な役割を担っているため、最大の市場シェアを占めている。この試験は規制遵守に不可欠であり、開発プロセスの早い段階で潜在的なリスクを特定するのに役立つ。医薬品の処方が複雑化し、精密医療への需要が高まっているため、堅牢な毒性試験の必要性がさらに高まっている。さらに、in-vitroおよびin-silico毒性学的手法の進歩が、同分野の成長を牽引している。
- 最終用途に基づいて市場は、バイオ製薬会社、政府および学術機関、医療機器会社に分けられますが、中でもバイオ製薬会社が市場を独占しているのは、生物製剤や新規治療法の有効性と安全性を確保するために前臨床試験に依存しているためです。研究開発への投資水準は高く、創薬と開発のあらゆる側面をカバーするサービスを必要としています。 モノクローナル抗体や遺伝子治療を含む生物学的製剤に対する需要の高まりも、その優位性を強固なものにしています。 専門の CRO 企業と契約を結ぶことで、バイオ医薬品企業は業務を合理化し、コストを削減し、市場シェアを拡大することができます。
| レポートの特徴 | 詳細 |
|---|---|
| 2024年の市場規模 | 64億米ドル |
| 2033年の市場予測 | 113億米ドル |
| 市場成長率 2025-2033 | 6.5% |
| 単位 | 億米ドル |
| レポートの範囲 |
歴史的傾向と市場の見通し、業界の促進要因と課題、セグメント別の歴史的および将来の市場評価の調査:
|
| 対象サービス | バイオアナリシスおよびDMPK試験、トキシコロジー試験、その他 |
| 対象となる最終用途 | バイオ製薬会社、政府・学術機関、医療機器会社 |
| 対象地域 | アジア太平洋、ヨーロッパ、北米、中南米、中東、アフリカ |
| 対象国 | アメリカ、カナダ、ドイツ、フランス、イギリス、イタリア、スペイン、ロシア、中国、日本、インド、韓国、オーストラリア、インドネシア、ブラジル、メキシコ |
| 対象企業 | Charles River Laboratories Inc., Covance Inc. (Laboratory Corporation of America Holdings), Eurofins Scientific, ICON Plc, MD Biosciences Inc. (MLM Medical Labs), Medpace, Parexel International Corporation, PPD Inc., Wuxi AppTec, など。 |
| カスタマイズの範囲 | 10% 無料カスタマイズ |
| 販売後のアナリスト・サポート | 10~12週間 |
| 配信形式 | PDFとExcelをEメールで送信(特別なご要望があれば、編集可能なPPT/Word形式のレポートも提供可能です。) |
Need more help?
- Speak to our experienced analysts for insights on the current market scenarios.
- Include additional segments and countries to customize the report as per your requirement.
- Gain an unparalleled competitive advantage in your domain by understanding how to utilize the report and positively impacting your operations and revenue.
- For further assistance, please connect with our analysts.

 Inquire Before Buying
Inquire Before Buying
 Speak to an Analyst
Speak to an Analyst
 Request Brochure
Request Brochure




.webp)




.webp)












